Nouvelles découvertes sur les polyphénols qui activent le SIRT1
Le SIRT1 est l’un des sept gènes sirtuines que l’on trouve chez les mammifères. Il a été démontré que le gène SIRT1 joue un rôle crucial dans le vieillissement, les inflammations, le cancer, la consommation d’énergie, ainsi que dans d’autres fonctions essentielles du corps humain. Pouvoir activer spécifiquement et de manière fiable le gène SIRT1 permettrait d’obtenir de nombreux effets bénéfiques sur la santé. Les chercheurs et l’industrie pharmaceutique ont donc cherché les petites molécules capables d’activer le gène SIRT1.
Le resvératrol, un polyphénol issu du raisin, fut l’un des premiers composés découverts en mesure d’activer le gène SIRT1, bien que le mécanisme de cette activation n’était pas clairement identifié. D’autres composés, avec une structure similaire au resvératrol, se sont également révélés capables d’activer le gène SIRT1. L’inhibition du SIRT1 pouvant permettre une thérapie contre certains cancers, les recherches ont également porté sur de petites molécules permettant d’inhiber le gène SIRT1.
Kahyo et al. ont examiné 36 composés polyphénoliques chalcone différents dans un essai in vitro pour constater leurs effets sur le gène SIRT1. Le test a permis de mesurer directement l’activité de la désacétylase du SIRT1 en présence des différents composés. Une culture cellulaire réalisée sur des cellules HEK293T (une lignée cellulaire immortalisée embryonnaire de rein humain couramment cultivées dans les laboratoires) a été utilisé afin étudier plus avant l’effet des composés sur le SIRT1. Dans les cultures cellulaires, l’activité du gène SIRT1 dans la désacétylation p53 a été mesurée in vitro dans des lysats cellulaires en provenance de cellules transfectées avec p53. Les cellules ont également été traitées avec les composés polyphénoliques chalcone et les effets directs des composés sur la croissance des cellules ont été mesurés.
Les différents composés testés par Kahyo et al. peuvent être classés en stilbènes, chalcones, flavanones et flavonols. Plusieurs composés connus, comme le resvératrol et le ptérostilbène, ont également été étudiés. D’autres composés inédits ont été synthétisés de novo pour l’expérience.
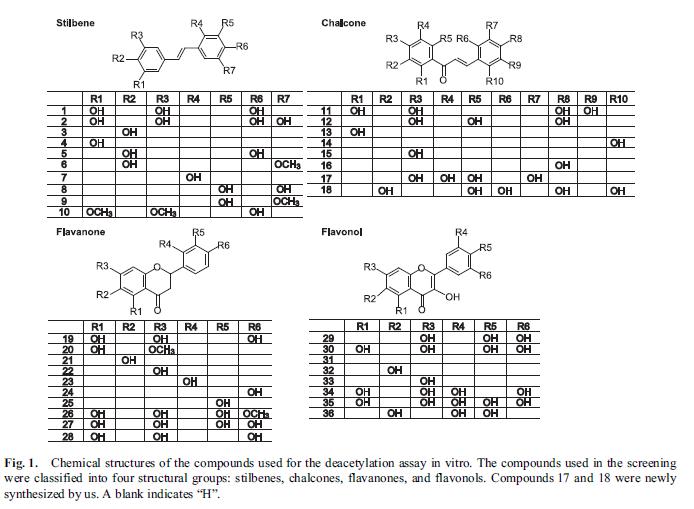
Trois des composés qui ont inhibé le gène SIRT1 in vitro ont été retenus pour poursuivre l’étude. Parmi ces trois composé, seul le 17 a pu inhiber directement la désacétylation de p53 dans le test de lysat cellulaire. Le composé 17 a été appliqué aux cellules HEK293T à dose relativement faible. Il peut inhiber la désacétylation de p53 in vivo, ce qui provoque une hyperacétylation de p53. Le traitement avec le composé 17 a inhibé la croissance des cellules.
Plusieurs composés bien connus ont été inclus dans cette étude. Le resvératrol est #1, le piceatannol #2, le ptérostilbène #10 et la quercétine #30. L’étude est particulièrement intéressante car elle mis en place un nouveau test pour l’activation de SIRT1 (le dosage de désacétylation de p53). Les résultats de l’étude de Kahyo et al. révèlent que le composé #1 (le resvératrol) n’active que marginalement le gène SIRT1 dans ce nouveau protocole de test. Le picéatannol (#2) et le ptérostilbène (#10) a activé le gène SIRT1 de façon plus importante que le resvératrol. On a longtemps cru que la quercétine, une flavanone, permettait d’activer le SIRT1 ; Toutefois, dans cette étude, elle s’est révélée être un puissant inhibiteur de SIRT1 in vitro.
Récemment, des études sur le mécanisme d’activation du gène SIRT1 par le resvératrol ont suggéré qu’il pourrait ne pas l’activer directement. En réalité, il semble simplement améliorer la désacétylation des peptides qui contiennent une modification du Fluor de Lys, provoquant un effet secondaire qui active le gène SIRT1. Une modification du Fluor de Lys consiste en la fixation d’une molécule fluorescente au peptide. Le picéatannol (#2) est un métabolite du resvératrol. Il est possible que de nombreux effets bénéfiques cliniquement constatés en réponse à la prise de resvératrol soient dû à sa décomposition par l’organisme en picéatannol, qui active alors directement le SIRT1. Dans la médiation de certains de ses effets bénéfiques démontrés, le resvératrol peut également agir sur d’autres gènes que le SIRT1.
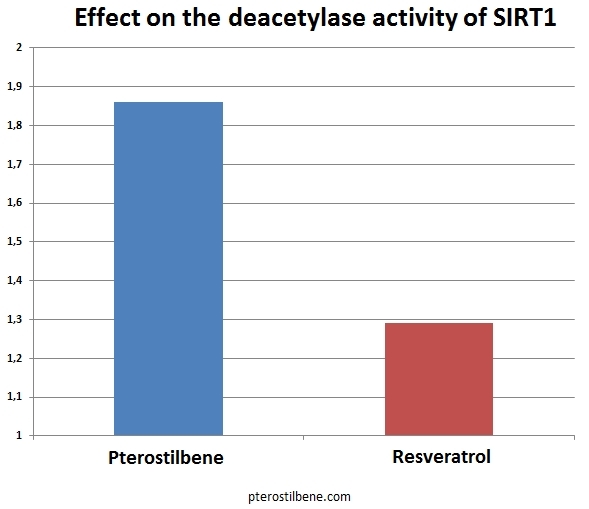
Le ptérostilbène (#10) est un stilbène avec une structure similaire au resvératrol. Dans la dernière étude en date, il a activé directement le SIRT1 dans une bien plus grande mesure que le resvératrol (avec respectivement 1,86 et 1,29 voir le graphique ci-dessus). Le pterostibène est connu pour être plus facilement absorbé par le corps et pour avoir une demi-vie beaucoup plus longue dans le corps que le resvératrol. Si le ptérostilbène a une plus grande capacité à activer directement le gène SIRT1, la combinaison d’une plus grande biodisponibilité et d’une plus grande activité pourrait donner au ptérostilbène des effets exponentiellement plus importants in vivo sur la santé. En plus de ses effets sur le SIRT1, le ptérostilbène s’est révélé être en mesure d’abaisser la glycémie aussi efficacement que la métaformine, de réduire le taux de cholestérol, et d’inhiber NF-kappa B, bloquant ainsi les voies inflammatoires.
Dans l’étude de Kahyo et al., ils expliquent que leur test pour l’activation du gène SIRT1 est mieux conçu et devrait donner des résultats plus précis. Dans les tests précédents, l’activité du quencher du substrat pouvait affecter les résultats des expériences. Dans le nouveau test, le fluorophore et le quencher sont fixés aux extrémités du substrat, ce qui empêche l’activité du quencher du substrat affecte les résultats du test. Des résultats antérieurs qui ont démontré que le resvératrol et la quercétine étaient de puissants activateurs de SIRT1 pouvaient être entièrement imputables à l’activation de l’activité du quencher dans les anciens tests.
Kahyo et al. ont activement recherché des agents inhibiteurs du gène SIRT1, et ont donc ignoré leurs conclusions sur les activateurs les plus puissants de SIRT1. Ils ont identifié quatre activateurs assez puissants de SIRT1 : le ptérostilbène, le picéatannol, et deux composés jamais étudiés auparavant. Les chercheurs qui s’intéressent à l’activation de SIRT1 pourrait vouloir se tourner vers ces quatre composés.
Puisque le picéatannol a permis d’observer le meilleur résultat (3,09), il est maintenant intéressant de le comparer avec le ptérostilbène.
Ptérostilbène et picéatannol : lequel choisir ?
Les études du groupe phénol contenant des molécules de stilbène comme le resvératrol et le picéatannol suggèrent qu’ils sont rapidement éliminés de l’organisme par le foie. Dans le foie, ils subissent une large glycuronidation (2) (3) (4). Peu de temps après l’injection intraveineuse, les formes d’acide glucuronique sont prédominantes, à la fois dans le plasma et dans l’urine comme cela avait été vérifié par des études de spectrométrie de masse in vivo réalisées sur l’homme.
Une fois que ce type de stilbène a été glucuroconjugué et a subit une sulfatation au niveau du foie et de l’intestin, il est rapidement excrété. La plus grande partie de l’excrétion semble se faire par les conduits biliaires, et une faible partie par l’urine. On peut raisonnablement conclure que la biodisponibilité des molécules de stilbène est indirectement proportionnelle à leur vitesse d’élimination hépatique. Le picéatannol, la pinosylivne et la rhapontigénine semblent tous être éliminé par l’organisme selon un taux maximal qui dépend uniquement du temps qui leur est nécessaire pour être transporté via la circulation sanguine vers le foie. Cela laisse penser que leur biodisponibilité est très limitée et qu’ils ont une demi-vie très courte dans le corps (2), ce qui limite grandement leur intérêt en tant que complément alimentaire.
D’autre part, les stilbènes qui ont remplacé les groupes fonctionnels phénol avec des groupes méthoxy, comme le ptérostilbène, ne peuvent pas subir de large glycuronidation (2). Ces stilbènes ont des pharmacocinétiques complètement différentes et ne sont pas éliminés rapidement par le corps après administration orale ou perfusion intraveineuse (5) (6). Ils ont une demi-vie longue et peuvent atteindre dans le corps des niveaux thérapeutiques après administration par voie orale une fois ou deux fois par jour. Avec le ptérostilbène, nous pouvons activer le gène SIRT1 plus efficacement qu’avec le resvératrol et plus longtemps qu’avec le picéatannol, ce qui en fait le meilleur complément alimentaire.
Référence:
(1)J Pharmacol Sci. 2008 Nov;108(3):364-71. Epub 2008 Nov 13.
(2) DOI 10.1211/jpp.58.11.00XX
(3) J. Pharmacol. Exp.Ther. 302: 369–373
(4) Mol. Nutr. Food Res. 49: 472–481
(5) Pharmacokinetics, oral bioavailability, and metabolic profile of resveratrol and its dimethylether analog, pterostilbene, in rats: I.M. Kapetanovic et al.; Cancer Chemother Pharmacol. (2010)
(6) Pharmacometrics of pterostilbene: preclinical pharmacokinetics and metabolism, anticancer, antiinflammatory, antioxidant and analgesic activity: C.M. Remsberg et al.; Phytother Res. 22, 169 (2008)

Leave a comment